Początki, czyli historia Gilgamesza
Wszystko zaczęło się w 1989 roku w małym niemieckim mieście. Nastoletni wówczas Steve Horvath, wraz ze swoim bratem bliźniakiem Markusem i ich znajomym Jörgem Zimmermanem, regularnie spotykali się by dyskutować o matematyce, fizyce i filozofii. Spotkania te często przeradzały się w rozważania nad tym jak nauka może przedłużyć ludzkie życie. Nazwali je ‘Projektem Gilgamesz’ od sumeryjskiego króla poszukującego tajemnicy nieśmiertelności. Na ostatnim spotkaniu, cała trójka postanowiła poświęcić swoje przyszłe naukowe kariery badaniom nad długowiecznością. Wybierając dalszą ścieżkę edukacji, Steve zdecydował się podejść to zagadnienie od strony matematycznej, a Jörg zajął się informatyką i sztuczną inteligencją. Nie wytrwał jedynie Markus, który został psychiatrą1.
Naukowcy i filozofowie interesowali się przedłużeniem życia od zawsze, lecz prawdziwy rozkwit badań przypadł na nastoletnie lata Horvatha. Rok przed powstaniem Projektu Gilgamesz, Robert Moyzis opublikował sekwencję ludzkiego telomeru – niewielkiej struktury DNA która znajduje się na końcu każdego chromosomu2. Telomery są niezbędne do prawidłowego funkcjonowania komórek – przy każdym podziale komórkowym chromosomy odrobinę się skracają, co, gdyby nie telomery, mogłoby prowadzić do uszkodzenia istotnych sekwencji DNA – na przykład genów. Gdy po wielu podziałach telomery osiągają krytycznie krótką długość, komórka przestaje się dalej dzielić, przechodząc na swojego rodzaju ‘emeryturę’ – ograniczenie to znane jest jako limit Hayflicka. Szybko okazało się, że obserwując długość telomerów można oszacować ilość podziałów, a zatem i “wiek” komórki. Posiadanie znacznika, który może nam powiedzieć, czy komórka starzeje się szybciej, czy wolniej niż powinna, szerzej otworzyło drzwi badaniom molekularnym nad czynnikami mogącymi przedłużyć życie, a z pewnością rozpaliło wyobraźnię wielu naukowców.
Intrygująca epigenetyka
W tym samym czasie naukowcy zainteresowali się epigenetyką – nauką o chemicznych i strukturalnych modyfikacjach genomu. Nie zmieniają one sekwencji DNA, lecz mogą wpłynąć na poziom ekspresji genów i są przekazywane kolejnym komórkom po podziale. Jedną z najlepiej zbadanych zmian epigenetycznych jest metylacja, która polega na dołączeniu grupy metylowej (-CH3) do cytozyny (jednej z czterech “liter” w naszym DNA), lecz tylko wtedy, gdy następuje po niej guanina (tak zwane “sekwencje postaci CpG”)*. W genomie ludzkim jest to modyfikacja niezwykle częsta – ponad 60% cytozyn w sekwencjach CpG, czyli około 40 milionów, jest zmetylowanych – i niezbędna do prawidłowego rozwoju i funkcjonowania organizmu. Prawdziwy przełom w badaniach nad epigenetyką pojawił się wraz z rozwojem wysokoprzepustowych mikromacierzy pozwalających na jednoczesne określenie stanu metylacji najpierw 27, a potem 450 tysięcy pozycji CpG w całym ludzkim genomie**.
Przełomowy moment
Dwadzieścia lat po rozpoczęciu projektu Gilgamesz, Steve Horvath pracował na University of California, Los Angeles. Jego współpracownik, Eric Vilain, próbował zbadać, czy różnice w preferencjach seksualnych między bliźniakami jednojajowymi mogą być wyjaśnione przez epigenetykę. Po pobraniu próbek od kilkudziesięciu par, zbadał i przeanalizował poziom metylacji na 27 tysiącach pozycji CpG, szukając różnic między bliźniakami. Nie udało mu się uzyskać jednoznacznych wyników, lecz podzielił się zbiorem danych z Horvathem. Ten z wielkim zdumieniem odkrył, że różnice w metylacji nie są być może związane z seksualnością, ale na ich podstawie, ze zdumiewającą dokładnością, jesteśmy w stanie przewidzieć wiek ludzi bliźniaków. Silna korelacja była dla niego tak wstrząsająca, że postanowił porzucić wszystkie projekty, którymi akurat wtedy zajmował się w laboratorium, i zająć się wyłącznie badaniami nad szacowaniem wieku z poziomu metylacji. Zaczął od śliny i mózgu, lecz później postanowił podnieść poprzeczkę i zebrał dane z wielu ludzkich tkanek, budując uniwersalny i wielotkankowy zegar epigenetyczny. Dzięki niemu, nieważne czy dysponujemy próbką krwi, wątroby czy płuca – jesteśmy w stanie oszacować wiek tej próbki,a nawet całego organizmu. W 2013 opublikował on swój algorytm, znany teraz jako Zegar Horvatha (ang. ‘Horvath Clock’)3.
Zegar Horvatha i jego działanie
Zegar Horvatha, czyli narzędzie wykorzystywane obecnie w badaniach nad długowiecznością i procesami starzenia, opiera się na przeanalizowaniu 353 pozycji CpG rozrzuconych po całym genomie, które mogą być zmetylowane lub nie, w zależności od naszego wieku (można to sobie wyobrazić jako ‘rdzewienie’ naszego DNA). Dysponując wzorem metylacji tych pozycji, Zegar Horvatha jest w stanie przewidzieć wiek organizmu z bardzo dużą dokładnością – zdecydowanie większą, niż wcześniejsze metody, wykorzystujące długość telomerów (50% wyników różniło się od wieku chronologicznego o mniej niż 3.6 roku). Od publikacji wyników badań nad zegarem Horvatha pojawiło się wiele innych wersji, również z innych laboratoriów, lecz to Horvath jest pionierem i liderem w ich ulepszaniu. Jednym z ciekawszych wynalazków jest zegar zmniejszony do jedynie trzech pozycji CpG – który mimo małego rozmiaru jest w stanie przewidzieć wiek wystarczająco dokładnie, aby być przydatnym na przykład w kryminalistyce4.
Zegary epigenetyczne wskazują wiek biologiczny, który może być mniejszy lub większy od wieku chronologicznego, w zależności od stanu zdrowia komórek. Horvath odkrył, że wiek biologiczny jest związany z ryzykiem chorób wieku starczego i z nowotworami. Ludzie o niższym wieku biologicznym żyją dłużej niż ich chronologiczni rówieśnicy, którzy są starsi biologicznie. Zauważył też, że kobiety są epigenetycznie młodsze od mężczyzn – co idzie w parze z dłuższą oczekiwaną długością życia u kobiet5.
Zegar w badaniach procesów starzenia
Odkrycie zegaru Horvatha pozwoliło na usprawnienie badań nad wieloma chorobami związanymi z wiekiem, jak również nad czynnikami i substancjami, które mogą nas “odmłodzić” lub spowolnić starzenie. Badanie opublikowane w 2017 roku pokazało, że czynniki które znacząco hamują starzenie to, między innymi, konsumpcja ryb częściej niż mięsa innych zwierząt, niskie spożycie alkoholu, odpowiednie BMI i regularne spożycie owoców i warzyw. Również regularnie uprawianie sportu miało znaczenie. Natomiast czerwone mięso, stres, wysokie BMI i niektóre choroby neurodegeneratywne wiążą się z kolei z wyższym wiekiem epigenetycznym, a zatem z przyspieszonym starzeniem (Diagram 1) 6.
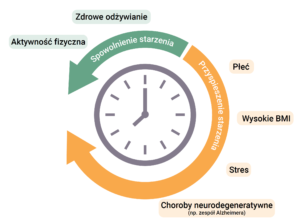
Diagram 1. Wpływ różnych czynników na proces starzenia. Aktywność fizyczna i zdrowe odżywianie go spowalniają, a płeć (mężczyźni starzeją się szybciej od kobiet), wysokie BMI, stres i niektóre choroby mogą go przyspieszyć. Diagram na podstawie Fig. 1 w Declerck i Berghe, 2018 7
Badania nad długowiecznością, na których wyniki wszyscy czekamy
W zeszłym roku, Gregory Fahy i współpracownicy opublikowali wyniki małej próby klinicznej, w której poprzez podanie mieszaniny hormonu wzrostu, metforminy i dehydroepiandrosteronu zdołali wydłużyć szacowaną długość życia uczestników o 1.5 roku8. Skąd uczeni wiedzieli jaka jest przewidywana długość życia? Jej kalkulator to kolejny wynalazek zespołu Horvatha, nazwany GrimAge (ponieważ wysoki wynik to ‘ponure’ (ang. grim) wieści). Brany jest w nim pod uwagę wiek epigenetyczny, jak również poziomy różnych białek we krwi i ilość spalonych papierosów. Czy półtora roku to niewiele? To tylko pierwszy etap badań, od czegoś trzeba zacząć! 😉
Specjalne zegary epigenetyczne, jak już wspomnieliśmy, mogą być też użyte w kryminalistyce – nie skupiają się one wtedy na odzwierciedleniu wieku biologicznego, lecz chronologicznego, by z dokładnością oszacować wiek ofiary czy sprawcy, czasem z bardzo małych, zdegradowanych tkanek – na przykład kropli krwi czy włosów pozostawionych na miejscu zbrodni.
Wyjątkowo: najpierw ludzie, potem myszy
Co ciekawe, mimo że większość badań farmakologicznych jest najpierw prowadzona na myszach, zegar epigenetyczny pozwalający na dokładne określenie ich wieku biologicznego pojawił się dopiero w 2017 roku, sześć lat po publikacji prototypu pierwszego ludzkiego zegara9. Powodem tego opóźnienia był brak mysiego odpowiednika tanich mikromacierzy do określenia poziomu metylacji – stworzenie zegara musiało poczekać na obniżenie kosztów innych metod badawczych, zwłaszcza sekwencjonowania. Dysponując mysim zegarem, naukowcy będą mogli dokładniej poznać wpływ badanych substancji na starzenie się całego organizmu, co nie jest możliwe w badaniach prowadzonych na liniach komórkowych i oczywiście może być niedozwolone w próbach klinicznych – w szczególności dla nowych substancji, które nie były wcześniej testowane na ludziach.
Nie rezygnuj z marzeń
Nastoletnie postanowienie i późniejsze przypadkowe (jak to często w nauce bywa) odkrycie Horvatha pozwoliło na przełom w badaniach nad procesem starzenia i w poszukiwaniu substancji przedłużających życie. Marzenia o długowieczności powoli stają się osiągalne, szczególnie dla wizjonerów takich jak Horvath. Jednak porzućcie nadzieje o nieśmiertelności. Według Horvatha, maksymalny wiek, który możemy osiągnąć w naszym gatunku, to około 123 lata. Lecz kto wie, co kiedyś przyniesie nauka?
* Metylacja może pojawiać się również na adeninach lub cytozynach w kontekście innym niż CpG – jest to jednak zmiana bardzo rzadka i ich wpływ na organizm ludzki nie jest jeszcze w pełni poznany.
** Obecnie dysponujemy bardziej nowoczesnymi metodami, które pozwalają nam określić stan metylacji prawie wszystkich pozycji CpG w genomie (najczęściej Whole Genome Bisulfite Sequencing – WGBS). Wraz z pojawieniem się nowych zbiorów danych z już nie 450 tysiącami, lecz 60 milionami pozycji CpG, naukowcy zaczęli badać, czy większy zestaw pozycji może udoskonalić zegary epigenetyczne. Co ciekawe, wcale tak nie jest! Początkowo wybrane 353 pozycje są na tyle informatywne, że dodanie kolejnych poprawia wyniki tylko o marginalne wartości. Tego samego nie można powiedzieć o cenie – mikromacierze są wciąż o wiele tańsze od WGBS.
Zegar epigenetyczny – matematyczne algorytmy, które używają wartości metylacji wcześniej ustalonych pozycji CpG aby określić wiek osoby lub próbki. Wielotkankowy zegar epigenetyczny pozwala na oszacowanie wieku jakiejkolwiek komórki, tkanki lub organu.
Wiek biologiczny – koncept oceniający biologiczny stan jednostki w porównaniu do średnich standardów w danej fazie życia.
Wiek chronologiczny – inaczej wiek kalendarzowy określający ilość czasu która minęła od punktu zero, czyli narodzin.
——————————–
1. Gibbs, W. W. Biomarkers and ageing: The clock-watcher. Nat. News 508, 168 (2014).
2. Blackburn, E. H., Greider, C. W. & Szostak, J. W. Telomeres and telomerase: the path from maize, Tetrahymena and yeast to human cancer and aging. Nat. Med. 12, 1133–1138 (2006).
3. Horvath, S. DNA methylation age of human tissues and cell types. Genome Biol. 14, R115 (2013).
4. Weidner, C. I. et al. Aging of blood can be tracked by DNA methylation changes at just three CpG sites. Genome Biol. 15, R24 (2014).
5. Horvath, S. & Raj, K. DNA methylation-based biomarkers and the epigenetic clock theory of ageing. Nat. Rev. Genet. 19, 371–384 (2018).
6. Quach, A. et al. Epigenetic clock analysis of diet, exercise, education, and lifestyle factors. Aging 9, 419–446 (2017).
7. Declerck, K. & Vanden Berghe, W. Back to the future: Epigenetic clock plasticity towards healthy aging. Mech. Ageing Dev. 174, 18–29 (2018).
8. Fahy, G. M. et al. Reversal of epigenetic aging and immunosenescent trends in humans. Aging Cell 18, e13028 (2019).
9. Stubbs, T. M. et al. Multi-tissue DNA methylation age predictor in mouse. Genome Biol. 18, 68 (2017).