Czym jest biopsja?
Współczesna diagnostyka wielu chorób nie może obyć się bez biopsji, czyli pobrania próbki materiału biologicznego z potencjalnie zmienionych tkanek. Próbka ta jest następnie poddawana szczegółowej ocenie lub innym, dedykowanym analizom. Geneza nazwy biopsja wywodzi się z języka starogreckiego i jest zlepkiem dwóch słów: bios, oznaczającego życie oraz opsis – obserwację. Pierwsze wzmianki o przydatności badania zmienionych chorobowo tkanek sięgają początku XI wieku, kiedy to arabski medyk Abulcasis, pobrał próbkę z wola tarczycy żyjącego pacjenta i następnie scharakteryzował ten wycinek tkanki.
Biopsja w formie, jaką znamy, została wprowadzana do praktyki medycznej dopiero w XIX wieku, przez francuskiego dermatologa, Ernesta Besniera. Szerokie stosowanie tej metody diagnostycznej w świecie klinicznym wymagało wcześniejszego upowszechnienia się procesu oceny mikroskopowej skrawków utrwalonych preparatów tkankowych, a także powstanie mikrotomów, niezbędnych do odpowiedniego pocięcia przygotowanych próbek.
Obecnie biopsja jest standardowym postępowaniem w diagnostyce całego szeregu chorób, począwszy od wrzodów, różnego rodzaju chorób zapalnych, po endometriozę i nowotwory. Biopsję wykonuje się w sytuacjach, gdy nie jest możliwe postawienie jednoznacznej diagnozy na podstawie objawów klinicznych lub w sytuacji, gdy potrzebne jest potwierdzenie postawionego rozpoznania przed rozpoczęciem właściwego leczenia. Najczęstszym zastosowaniem biopsji jest wykluczenie lub potwierdzenie zmian o charakterze nowotworowym.
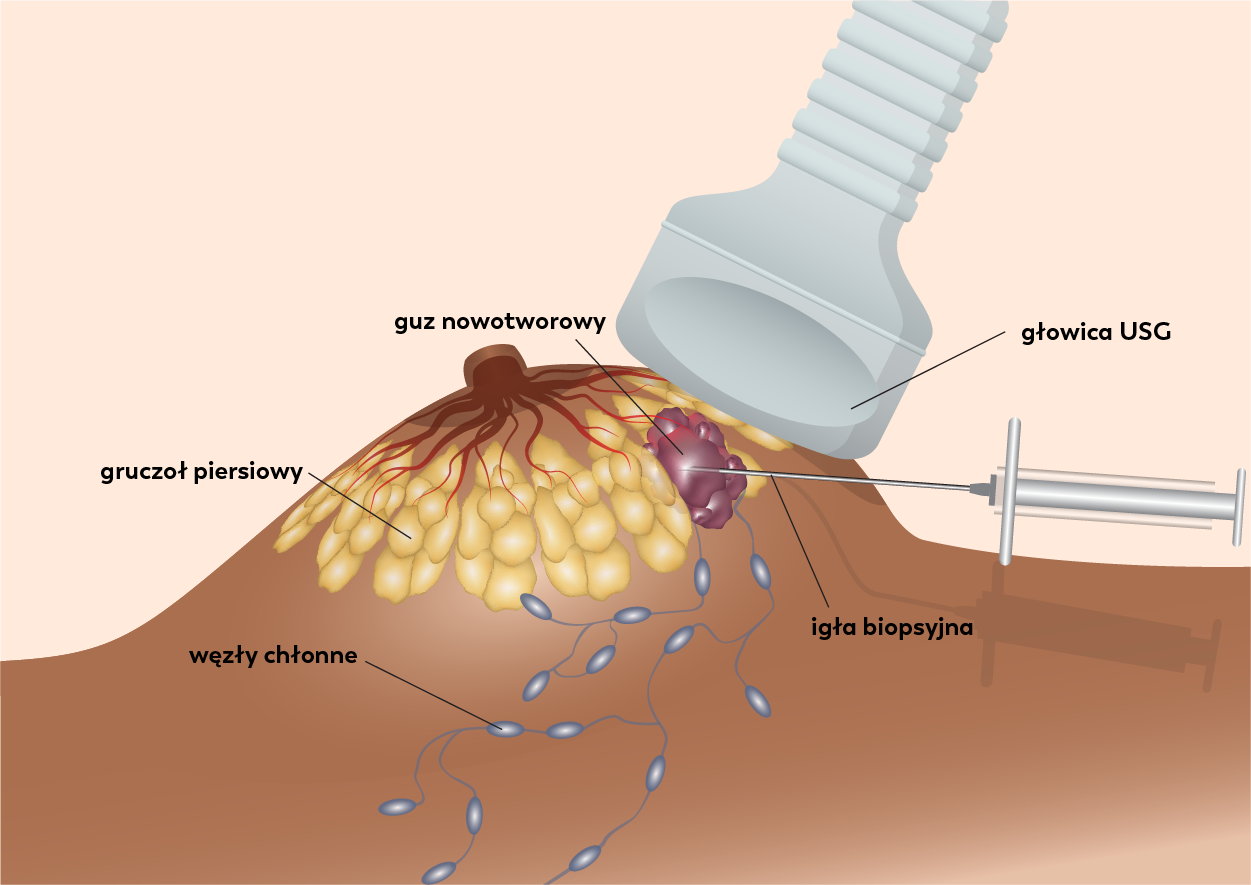
Rycina 1. Grafika przedstawiająca biopsję gruboigłową piersi wykonywaną pod kontrolą aparatu USG.
Rodzaje biopsji
Istnieje cały szereg różnego rodzaju biopsji wykonywanych w ramach procedur medycznych:
- Biopsja szczoteczkowa – jest to wymaz wykonywany za pomocą specjalnej szczoteczki. Polega ona na pobraniu materiału komórkowego z powierzchni nabłonka np. wyściełającego szyjkę macicy lub drogi oddechowe.
- Biopsja aspiracyjna cienkoigłowa (BAC) – biopsja wykonywana poprzez zassanie (aspirację) komórek z badanej tkanki do bardzo cienkiej igły (ok. 0.6 mm), wkłutej w podejrzaną zmianę.
- Biopsja gruboigłowa – podobnie jak w przypadku BAC, tu również wykorzystywana jest igła do pobrania materiału z tym, że jest to igła o większej średnicy (ok. 1.2-2 mm). (Ryc. 1). Pozwala ona na pobranie niewielkiego wycinka zmienionej tkanki, a nie tylko luźnych komórek, co daje znacznie większe możliwości oceny patomorfologicznej materiału. Specjalną modyfikacją biopsji gruboigłowej, dedykowaną do diagnostyki raka piersi jest biopsja mammotoniczna (zwana również próżniową). Dzięki zastosowaniu grubej igły (ok. 3 mm średnicy) z ruchomym ostrzem wewnątrz i podłączonej pompie próżniowej, umożliwia ona pobranie licznych wycinków, lub nawet całkowite usunięcie zmiany, przy jednorazowym wkłuciu w powłoki skórne.
- Biopsja wyskrobinowa – szczególnie często stosowana w ginekologii, w czasie której lekarz za pomocą specjalnej łyżki wyskrobuje zawartość jamy macicy i pobiera pasemka tkankowe do dalszej analizy.
- Biopsja chirurgiczna jest bardziej inwazyjną formą biopsji, którą możemy podzielić na:
- biopsję wycinkową, gdzie za pomocą skalpela lub sztancy pobierany jest wycinek ze zmiany (Ryc. 2),
- biopsję wycinającą, gdzie zmiana jest wycinana w całości wraz z marginesem zdrowej tkanki.
- biopsja wykonana za pomocą laparoskopu lub endoskopu, co minimalizuje inwazyjność zabiegu w porównaniu do otwartego, tradycyjnego zabiegu chirurgicznego.
Zarówno biopsja cienkoigłowa, jak i gruboigłowa, mogą być wykonywane ze wsparciem różnych metod obrazowania, takich jak USG, tomograf komputerowy, rezonans magnetyczny czy badanie radiologiczne (biopsja stereotaktyczna). Dzięki temu lekarz może precyzyjnie dotrzeć do zmian niewyczuwalnych badaniem palpacyjnym lub zlokalizowanych w głęboko umieszczonych tkankach np. zmiany w nerce lub wątrobie).

Rycina 2. Sztance biopsyjne w różnych rozmiarach do pobierania wycinków.
Biopsja płynna
Osobnym, istotnym podtypem biopsji, jest tzw. biopsja płynna. Ma ona zastosowanie w onkologii, choć nie jest procedurą powszechnie stosowaną. Badanie to polega na wykryciu we krwi pobranej od pacjenta krążących komórek nowotworowych (CTC – Circulating Tumour Cells). Następnie analizie poddaje się obecność charakterystycznych antygenów na powierzchni komórek nowotworowych. Mogą to być komórki, które oddzieliły się od guza pierwotnego lub też komórki nowotworów krwi, krążące swobodnie w krwi obwodowej. Badanie biopsji płynnej wykonywane jest w celu monitorowania efektów leczenia lub wczesnego wykrywania wznowy. W trakcie leczenia ilość krążących komórek nowotworowych powinna ulegać zmniejszeniu, jeśli pozostaje ona na niezmienionym poziomie może to świadczyć o nieskuteczności lub oporności na dotychczasowe leczenie.
W ramach płynnej biopsji możliwe jest również wykonywanie analizy DNA z krążących komórek nowotworowych (circulating tumor DNA, ctDNA). Pozwala ono na identyfikację celów molekularnych do terapii personalizowanej, jednak metoda ta nadal jest obarczone dużym ryzykiem otrzymania fałszywych wyników lub niewykrycia istotnych klinicznie zmian i w ostatnim czasie spotkało się z dużą krytyką środowiska medycznego [1].
Co się dzieje z materiałem pobranym w trakcie biopsji?
Bioptat, czyli próbka pobrana w ramach biopsji, trafia do laboratorium patomorfologicznego. Tam, gdy zachodzi potrzeba szybkiego potwierdzenia charakteru zmiany, wykonywane jest badanie śródoperacyjne preparatu, a reszta próbki jest zabezpieczana poprzez mrożenie lub poprzez utrwalenie w roztworze formaldehydu i zatopienie w parafinie. Lekarz patomorfolog po przygotowaniu skrawków lub rozmazów przeprowadza obserwację mikroskopową tych preparatów. W zależności od tego, czy mamy do czynienia z pobranymi komórkami np. w czasie biopsji aspiracyjnej cienkoigłowej, mówimy o badaniu cytologicznym; w przypadku preparatu tkankowego – o badaniu histopatologicznym. W czasie analizy oceniany jest m.in. kształt i typ komórek, architektura tkanek, a także morfologia zmian w nich zachodzących. Patomorfolodzy dysponują całą gamą narzędzi ułatwiających ocenę czy mają do czynienie ze zmianami o charakterze zapalnym czy mającymi podłoże nowotworowe. Wykorzystują między innymi różnego rodzaju barwienia cyto- i histochemiczne, które pozwalają uwidocznić konkretne cechy komórek lub typy zmian (Ryc. 3).
W przypadku potwierdzenia diagnozy choroby nowotworowej, badanie patomorfologiczne pozwala na dodatkowe określenie stopnia zaawansowania histologicznego raka tzw. grading [2]. Najczęściej wykorzystywana jest w tym celu skala od 1 do 4. Nowotwory niskiego stopnia (stopień 1) są na wczesnym etapie rozwoju i najczęściej są najmniej agresywne, nowotwory wyższego stopnia (stopień 4) są na ogół najbardziej agresywne i wiążą się z obecnością odległych przerzutów. Te informacje mogą pomóc w określeniu metody leczenia i dopasowaniu terapii.

Rycina 3. Gotowe do analizy histopatologicznej wybarwione skrawki z bloczków parafinowych.
Diagnostyka genetyczna
Poza technikami mikroskopowymi ogromne znaczenie, szczególnie w diagnostyce chorób nowotworowych, mają badania genetyczne preparatu tkankowego. Badania te wykrywają patogenne zmiany (mutacje) somatyczne, czyli zmiany, które powstały w komórkach w trakcie ewolucji nowotworu. Mutacje te mogą by wykrywane za pomocą różnych technik biologii molekularnej – wykrywania pojedynczych wariantów genetycznych metodą PCR, sekwencjonowania całych genów lub paneli wielu genów metodą NGS, a także sekwencjonowania całego genomu nowotworowego. Wykrycie konkretnych mutacji, jak BRAF V600E w czerniaku i raku jelita grubego czy też uszkodzeń całych genów np. BRCA1 lub BRCA2 w nowotworach jajnika, może być wskazaniem do stosowania konkretnych leków celowanych jak, kolejno, debrafenib czy leki z grupy inhibitorów PARP.
Metodą, które niewątpliwie zdominuje badania genetyczne materiału tkankowego pochodzenia nowotworowego w najbliższej przyszłości, jest profilowanie genetyczne guza, wykonywane przy użyciu obszernych paneli genowych czy też za pomocą najbardziej precyzyjnego i uniwersalnego badania – sekwencjonowania całego genomu [3]. Badania te już stają się standardem krajach z dobrze rozwiniętą służbą zdrowia, niestety w Polsce nadal żaden mechanizm finansowania opieki zdrowotnej nie przewiduje refundacji ich kosztu.
Czy cała próbka pobrana w czasie biopsji trafia do badania patomorfologicznego?
W przypadku pobrania dużej ilości materiału np. przy użyciu biopsji mammotonicznej, lekarz patomorfolog lub chirurg przeprowadzający zabieg może zdecydować o umieszczeniu części w biobanku. Pobrany wycinek zostaje wówczas zabezpieczony w specjalnym buforze i zamrożony. Tak przechowywana tkanka może być później wykorzystana do badań naukowych np. związanych z rozwojem nowych leków onkologicznych i metod diagnostycznych. Na świecie istnieją setki biobanków począwszy od niewielkich biobanków uniwersyteckich, skupiających się na zbieraniu próbek do realizacji konkretnych projektów, po gigantyczne biobanki, jak biobank w austriackim mieście Graz [4], w którym przechowuje się około 20 milionów pojedynczych próbek. Istnieją również biobanki komercyjne jak Polskie Centrum Biobankowania [5], które pozwalają pacjentom na przechowanie tkanki do dalszej, zaawansowanej diagnostyki. Taka forma zabezpieczenia tkanki jest istotna szczególnie w chorobach nowotworowych, gdzie w trakcie leczenia często dochodzi do oporności na dotychczas stosowany lek i trzeba szukać alternatyw, a dostęp do tkanki zmienionej nowotworowych jest często możliwy tylko raz.
Źródła:
- Liquid biopsy: misplaced faith in early cancer detection? https://www.statnews.com/2021/08/31/liquid-biopsy-misplaced-faith-in-early-cancer-detection/?fbclid=IwAR3zzgt9ZTPdVMR2YZAfWnFEdLusfC7SiA6W1ika7TiM5zWzn7nxKkdTZiE
- https://www.cancer.gov/about-cancer/diagnosis-staging/staging
- Molecular profiling of advanced solid tumours. The impact of experimental molecular-matched therapies on cancer patient outcomes in early-phase trials: the MAST study: https://pubmed.ncbi.nlm.nih.gov/34493820/
- https://biobank.medunigraz.at/
- https://pcbb.pl/







